Lasst die Trips in Ruhe
EIN NEUROWISSENSCHAFTLICHES PLÄDOYER GEGEN NICHT-HALLUZINOGENE PSYCHEDELIKA
Übersetzt von Martin Gürster, editiert von Lucca Jäckel

Editiert von Abigail Calder & Lucca Jaeckel
Disclaimer: Dieser Blogpost wurde von Volontären übersetzt und editiert. Die Mitwirkenden repräsentieren nicht die MIND Foundation. Wenn Ihnen Fehler oder Unklarheiten auffallen, lassen Sie es uns bitte wissen – wir sind für jede Verbesserung dankbar (mailto:[email protected]). Wenn Sie unser Projekt zur Mehrsprachigkeit unterstützen wollen, kontaktieren Sie uns bitte um der MIND Blog Translation Group beizutreten!
Die Frage, ob der “psychedelische Trip” für den therapeutischen Nutzen von Psychedelika wirklich notwendig ist, ist zum Gegenstand heftiger Debatten geworden. Diese Tatsache wird am besten durch zwei aktuelle, gegensätzliche Veröffentlichungen veranschaulicht: Einerseits von der Forschungsgruppe um Dr. David B. Yaden und Prof. Roland Griffiths,1 die für die Wichtigkeit der psychedelischen Erfahrung plädiert, gegenüber Dr. David Olson,2 welcher die Überzeugung vertritt, wir könnten (und sollten sie möglicherweise) verwerfen. Dieser Beitrag gibt ein neurowissenschaftlich fundiertes Argument, warum wir die subjektive Erfahrung nicht ignorieren sollten.
Eine aktuelle Veröffentlichung aus dem Labor von Dr. David Olson an der University of California, Davis, die ein nicht-halluzinogenes Derivat der psychedelischen Substanz Ibogain beschreibt, genannt Tabernanthalog (TBG), hat Ende 2020 in der psychedelischen Forschungsgemeinschaft viel Aufsehen erregt.3 Von Ibogain ist bekannt, dass es antidepressive und suchthemmende Eigenschaften hat, allerdings ist seine Verwendung durch ein ungünstiges Sicherheitsprofil eingeschränkt, welches Übelkeit, kardiologische Komplikationen4 und eine mögliche Wirkungsdauer von mehr als 24 Stunden beinhaltet.5 TBG hingegen hat gezeigt, dass es die therapeutischen Effekte von Ibogain in Mäusen ohne die damit verbundenen Risiken ermöglicht. Am wichtigsten ist aber, dass es dieses Molekül in die Schlagzeilen verschiedener Wissenschaftsmagazine geschafft hat, weil Erkenntnisse an Studien mit Mäusen nahelegen, dass TBG keinerlei halluzinogenen Eigenschaften besitzt. Obwohl es angeblich Trip-frei ist, hat sich gezeigt, dass TBG die Neuroplastizität im Kortex von Mäusen erhöht, genau wie sein psychoaktives Gegenstück Ibogain. Im Vergleich der Effekte von Ibogain mit denen von TBG könnte es Wissenschaftlern möglich werden, eine brisante Frage der psychedelischen Forschung zu beantworten: Können therapeutische Effekte ohne die subjektiven Wirkungen auftreten? Wenn klassische Psychedelika die Neuroplastizität erhöhen und durch Entündungshemmung gar eine antidepressive Wirkung erzielen, ist der Trip dann überhaupt notwendig?
Psychoplastogene [griechisch psyche- (Seele), -plast (geformt) und -gen (erzeugen)]: Kleine Moleküle, die eine messbare Veränderung der Neuroplastizität (z.B. Veränderungen des Neuritenwachstums, der dendritischen Stacheldichte, der Synapsenanzahl, der intrinsischen Erregbarkeit usw.) innerhalb kurzer Zeit (typischerweise 24-72 Stunden) nach einmaliger Verabreichung hervorrufen und zu relativ lang anhaltenden Verhaltensänderungen führen können.6
Obwohl fast alle identifizierten Psychoplastogene (z.B. Psilocybin, DMT, Ketamin, Scopolamin) psychoaktiv sind, ist diese Eigenschaft nicht Teil ihrer Definition. Der Grund dafür ist, dass einige Wissenschaftler inzwischen der Überzeugung sind, dass die Neuroplastizität auch ohne subjektive Erfahrung schnell stimuliert werden kann, was zu einer antidepressiven Wirkung führt.
Ein besonders effektiver Weg zur Stimulation von Neuroplastizität ist der Serotonin-2A-Rezeptor (5-HT2AR),7 der auch für die halluzinogenen Effekte von Psychedelika Voraussetzung ist.8,9 Jahrzehntelang galten Medikamente, die den 5-HT2AR stimulieren, als hochgradig risikobehaftet, Halluzinationen zu erzeugen, was ihre Entwicklung stark bremste. Jüngste theoretische Fortschritte in der Pharmakologie deuten jedoch darauf hin, dass Neuroplastizität und psychedelische Erfahrung möglicherweise doch nicht zusammengehören.10 Um das zu verstehen, müssen wir einen Blick in das Neuron selbst wagen und einen Prozess verstehen, der als “Biased Agonism” bezeichnet wird.
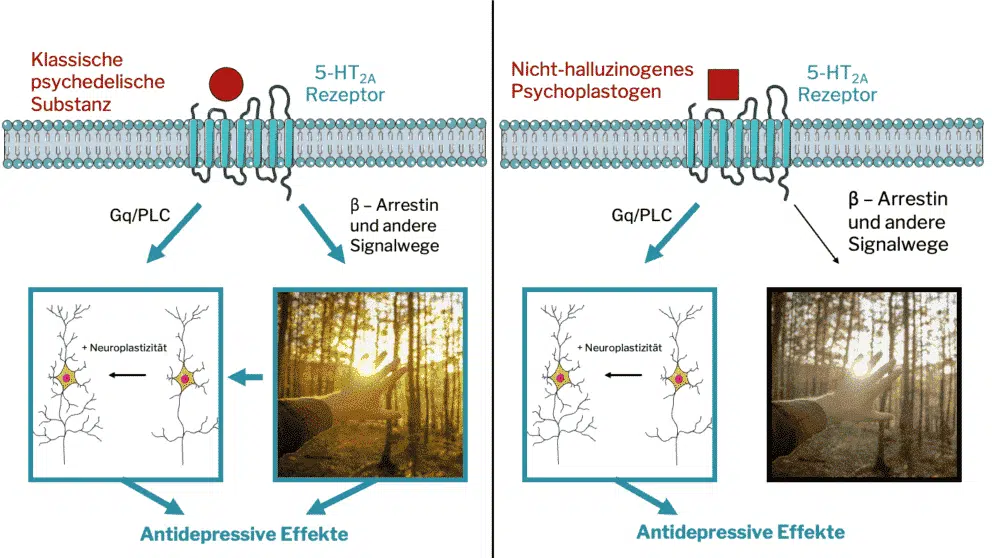
Abbildung 1: Mögliche therapeutische Mechanismen von (nicht-halluzinogenen) Psychedelika auf zellulärer Ebene. Auf der linken Seite wird die antidepressive Wirkung klassischer Psychedelika sowohl durch die psychoplastogene als auch durch die subjektive Wirkung erreicht, wobei unterschiedliche Signalwege genutzt werden; auf der rechten Seite wird die antidepressive Wirkung eines nicht-halluzinogenen Psychoplastogens nur durch Steigerung der Neuroplastizität erreicht; die zweite Substanz ist ein “Biased Agonist” – sie aktiviert bevorzugt den Gq/PLC-Pfad, wodurch die subjektive Wirkung umgangen – oder zumindest stark reduziert – wird.
Wenn ein Medikament an einen Rezeptor auf einer Zelle bindet, wird eine Reihe von biochemischen Kettenreaktionen (auch Signalwege genannt) im Inneren des Neurons ausgelöst.11 Jede dieser Reaktionen hat einen anderen Endpunkt; dies könnte die Produktion eines neuen Proteins oder eine Veränderung der elektrischen Aktivität sein, die wiederum zu komplexen Veränderungen führen, wie z. B. die Modifizierung der Kommunikation zwischen verschiedenen Hirnarealen und die Herstellung neuer Verbindungen zwischen Neuronen. Wenn ein “Biased Agonist” einen Rezeptor bindet, aktiviert er bevorzugt eine oder mehrere dieser Reaktionen zum Nachteil der anderen.10
Im Fall des 5-HT2A-Rezeptors gibt es drei wichtige Signalwege innerhalb des Neurons: Den Gq/PLC-, den PLA2- und den Beta-Arrestin-Weg.10,12 Obwohl die Details nicht ganz klar sind, können alle kognitiven und neurobiologischen Effekte, die der 5-HT2AR-Aktivierung zugeschrieben werden (von visuellen Halluzinationen bis zur Neuroplastizität), auf einen oder mehrere dieser Signalwege zurückgeführt werden. Ein voreingenommener Agonist könnte z.B. den Gq/PLC-Signalweg aktivieren, ohne die anderen beiden zu beeinflussen. In einem idealen Szenario liegen die psychoplastogenen Effekte am Ende des einen Signalwegs, während die halluzinogenen Effekte an einem anderen liegen. Einige Hinweise deuten darauf hin, dass dies tatsächlich der Fall sein könnte: Eine kürzlich erschienene Publikation kommt zu dem Schluss, dass Beta-Arrestin 2 für die “psychedelisch-ähnlichen” motorischen Effekte erforderlich ist, die bei Mäusen beobachtet wurden (d.h. Kopfzuckungen, rückläufiges Gehen, Nasenstochern).13 Ergänzend dazu wurde zuvor gezeigt, dass Neuroplastizität mit dem Gq/PLC-Signalweg verbunden ist,14,15 der ebenfalls einen reduzierten Einfluss auf “psychedelisch-ähnliche” motorische Effekte bei Mäusen zu haben scheint.16 Schließlich wird der Gq/PLC-Signalweg auch durch Lisurid, einem nicht-halluzinogenen Verwandten von LSD, aktiviert, was weiter darauf hindeutet, dass die subjektiven Effekte woanders liegen.17
Es besteht ein gewisser Konsens darüber dass subjektiv-positive psychedelische Erfahrung größeren therapeutischen Nutzen bringen kann, wie zu sehen in der beherzten Debatte zwischen Yaden und Olsen, die dieser Forschungsfrage eine Struktur gaben. Nichtsdestotrotz versuchen Wissenschaftler in der psychedelischen Industrie eine Verbindung zu entwickeln, die einen Teil des therapeutischen Potenzials beibehält, aber auch skalierbar und vermarktbar ist und an Menschen verabreicht werden kann, die durch den Screening-Prozess für eine psychedelische Erfahrung ausgeschlossen würden. TBG scheint ein starker Kandidat als weithin verabreichbares nicht-halluzinogenes Psychoplastogen zu sein. Aber wird es seinem Hype wirklich gerecht?
Also betrachten wir diese Verbindung eingehender, beginnend mit ihrer auffälligsten Besonderheit: dem Fehlen halluzinogener Eigenschaften. Die meisten tierexperimentellen Studien zum halluzinogenen Potenzial von Psychedelika basieren auf der Kopfzuckungsreaktion bei Mäusen. Diese gilt als Goldstandard für die Bewertung psychoaktiver Wirkung klassischer Psychedelika bei Mäusen, da mehrere Studien eine Korrelation zwischen der Bindung einer Substanz an den 5-HT2AR, der Intensität der Halluzinationen beim Menschen und der Kopfzuckungsreaktion gezeigt haben.18,19,20 Abgesehen von dem offensichtlichen Problem, dass eine Kopfbewegung weit davon entfernt ist, ein Einblick in das subjektive Erleben einer Maus zu s, gibt es jedoch einige wichtige Einschränkungen, die es zu erwähnen gilt.
In der Veröffentlichung zu TBG wird gezeigt, dass eine hohe Dosis Ibogain ebenfalls keinen statistisch signifikanten Anstieg der Kopfzuckungen hervorruft, was auch mit einer früheren Studie übereinstimmt.21 Dennoch ist Ibogain beim Menschen unbestreitbar halluzinogen.4 Darüber hinaus erzeugt die Serotonin-Vorstufe 5-HTP bei Mäusen eine starke Kopfzuckungsreaktion,22, 23 während sie beim Menschen psychologisch inaktiv ist. Das bedeutet, dass bis zur Einnahme von TBG durch einen Menschen keine definitiven Aussagen über die halluzinogenen Eigenschaften dieser Verbindung gemacht werden können, noch kann man die Existenz eines therapeutisch brauchbaren nicht-halluzinogenen Psychoplastogens per se annehmen. TBG ist nicht der erste Versuch in dieser Richtung, denn andere in Betracht gezogene Psychoplastogene, die eng mit Ketamin verwandt sind, haben sich entweder als psychoaktiv (Traxoprodil) oder als unwirksam in der Behandlung menschlicher Depressionen erwiesen (AZD6765, Rapastinel).24
Aktuell gehen wir davon aus, dass diese Verbindung beim Menschen tatsächlich nicht halluzinogen ist. Bei genauer Lektüre des TBG-Artikels3 zeigt sich, dass die maximale Aktivierung des Gq/PLC-Signalwegs (d.h. des Signalwegs, der eher mit Neuroplastizität als mit Halluzinationen in Verbindung gebracht wird) des 5-HT2A-Rezeptors durch TBG fast halb so groß ist wie die von Ibogain, 5-MeO-DMT (einem weiteren potenten Halluzinogen) und Serotonin selbst. Erinnern wir uns an das hypothetische Beispiel aus dem vorangehenden Abschnitt: Ein ideales nicht-halluzinogenes Psychedelikum würde den intrazellulären Weg, der zu einem psychedelischen Trip führt, nur minimal aktivieren, während es zugleich Neuroplastizität stark stimuliert. TBG könnte dem einen oder anderen Pfad am 5-HT2AR Vorzug gewähren oder auch nicht, aber aufgrund seiner intrinsischen Eigenschaften könnte es sein, dass es einfach nicht in der Lage ist, einen dieser Pfade in demselben Ausmaß zu aktivieren wie sein halluzinogenes Gegenstück Ibogain. Das würde bedeuten, dass eine hohe Dosis TBG die 5-HT2ARs schwach stimuliert, ähnlich wie eine Mikrodosis DMT, von dem auch gezeigt wurde, dass es bei Mäusen einige antidepressive und anxiolytische Effekte hervorruft.25
TBG könnte ein Milliarden-Dollar-Molekül sein – es ist patentiert, es könnte sowohl Depressionen als auch Sucht behandeln, es wird in einem Schritt synthetisiert, und es erspart Menschen möglicherweise den ‘psychedelischen Trip’, selbst wenn sie höhere Dosen einnehmen (einen ausführlichen kritischen Blick auf die kommerziellen Anreize für solche Verbindungen finden Sie in diesem Artikel im APRA-Blog). Aus pharmakologischer Sicht scheint TBG jedoch nicht viel anders zu sein als bereits existierende Lösungen. Und obwohl die Autoren der TBG Veröffentlichung einen Perspektivwechsel in der psychiatrischen Versorgung von der Korrektur “chemischer Ungleichgewichte” hin zur Korrektur “beschädigter Schaltkreise” betonen,6 wird die subjektive menschliche Erfahrung mit keinem Wort erwähnt, was den Anschein erweckt, dass dies nicht die Art von Paradigmenwechsel ist, den einige Praktizierende fordern.26
Nachdem wir nun die Neurobiologie von nicht-halluzinogenen Psychoplastogenen erforscht haben, wollen wir zum Kernpunkt der Neuroplastizität selbst kommen. Neuroplastizität ist in letzter Zeit zu einem Schlagwort in der psychedelischen Forschung geworden, wobei viele den therapeutischen Nutzen sowohl neuartiger (z.B. Ketamin, Psilocybin) als auch klassischer Antidepressiva (selektive Serotonin-Wiederaufnahmehemmer wie Fluoxetin) darauf zurückführen.27 Aber kann eine Steigerung der Plastizität allein die Aufgabe erfüllen, das Bewusstsein zu verändern?
Zunächst einmal: Was ist überhaupt Plastizität? Grob gesagt, ist es die Fähigkeit des Gehirns, seine Struktur und seine Funktionen durch Gehirnaktivität zu verändern. Konkret ist Neuroplastizität ein Überbegriff, der mehrere dynamische Prozesse umfasst, die verändern, wie Neuronen miteinander kommunizieren.28 In einer Hardware-Software-Analogie des Gehirns und des Geistes würde Neuroplastizität die Prozesse darstellen, durch die die Software (Gehirnaktivität) die Hardware (neuronale Schaltkreise) verändert.29 Zu diesen Prozessen gehören die Veränderung der Stärke bestehender Verbindungen, die Schaffung neuer Verbindungen (über neu gewachsene neuronale Verzweigungen, Dendriten genannt) und die Beseitigung alter Verbindungen.
Einige ExpertInnen glauben, dass Menschen Depressionen durch einen pathologischen Verlust von Verbindungen entwickeln, vor allem im präfrontalen Kortex,27,7 und dass Psychoplastogene diese Schaltkreise reparieren oder wieder ins Gleichgewicht bringen können.6 Was in diesem speziellen Diskurs selten betont wird, ist die Tatsache, dass das Gehirn ein hochgradig organisiertes, hierarchisches Organ ist. Das bedeutet, dass jede Verbindung eine präzise Funktion und Bedeutung hat, und dass Plastizität (genau wie die Gehirnaktivität selbst) kein zufälliger Prozess ist, sondern eine sorgfältig orchestrierte Kaskade, in der nützliche Verbindungen verstärkt werden und veraltete oder überflüssige verkümmern. Wichtig ist, dass die Nützlichkeit dieser Verbindungen lokal bewertet wird, durch Prinzipien der Homöostase und harmonischen Aktivität, und möglicherweise nur schwach mit guter Stimmung, Glück oder Erfüllung korreliert. Die Evolution hat unser Nervensystem wahrscheinlich eher für Funktionieren und Überleben als für psychologisches Wohlergehen optimiert. Es ist daher unwahrscheinlich, dass sich das Gehirn von selbst auf diese positiven Gefühle einstellt, durch bloße zelluläre Prozesse, die auf unspezifische Weise ausgelöst werden.Was genau können solche Psychoplastogene also wiederherstellen? Zunächst ist es wichtig zu beachten, dass die Eliminierung von Verbindungen, die nicht (mehr) hilfreich sind, mindestens genauso wichtig wie die Herstellung neuer Verbindungen ist. Einfach mehr Verbindungen herzustellen ist also nicht notwendigerweise hilfreich. Dr. David Olson, Leiter der Forschungsgruppe, welche den Begriff Psychoplastogen maßgeblich geprägt und TBG entwickelt hat, sagte dazu, dass „die hilfreichsten Psychoplastogene […] diejenigen sein [werden], die Plastizität in spezifischen Schaltkreisen verstärken können. […] Die willkürliche Förderung der Neuroplastizität wird wahrscheinlich nicht nützlich sein.“6 Worauf es also wirklich ankommt ist, welche Verbindungen gebildet oder gekappt werden sowie die Langlebigkeit dieser Veränderungen. Sogar in dem bahnbrechenden Fachartikel von Ly et al.7 (siehe MIND Blog Post), der die Assoziation von Psychedelika mit Neuroplastizität maßgeblich geprägt hat, heißt es, dass es noch unklar sei, wie lange die von Psychoplastogenen geschaffenen neuen Verbindungen bestehen bleiben, geschweige denn was sie bedeuten.
Plastizität tritt gewöhnlich infolge kohärenter neuronaler Aktivität auf, wie das bekannte Zitat des Neuropsychologen Donald Hebb besagt: „Neuronen die zusammen feuern, verknüpfen sich“ [Neurons that fire together, wire together]. Psychedelika und Ketamin scheinen diesen Prozess zu stärken, indem sie vorübergehend ein Fenster für die Zunahme an Plastizität eröffnen, dem direkt vorausgehend ein Strom von Gedanken, Emotionen und bildlichen Vorstellungen auftritt, unter denen einige einem bedeutungsvollen subjektiven Narrativ zu folgen scheinen.37
Es wurde gezeigt, dass solch interpersonelle Erfahrungen, sogenannte mystische Erfahrungen und auch persönliche Erkenntnisse während eines psychedelischen Trips mit der Langlebigkeit therapeutischer Effekte bei PatientInnen zusammenhängen.1, 30, 31, 32 Interessanterweise ist es außerdem scheinbar das Vorhandensein sowie die Stärke einer solchen mystischen Erfahrung – und nicht die allgemeine Intensität der subjektiven Erfahrung – welche mit den therapeutischen Effekten in Verbindung gebracht wird.1
Darüber hinaus ist die Effektivität MDMA-assistierter Psychotherapie für die Behandlung posttraumatischer Belastungsstörung auch stark davon abhängig, wie das therapeutische Setting gestaltet ist und welche Erfahrungen auf die akute Behandlung folgen. Dies könnte für einen Zeitraum von mindestens zwei Wochen gelten, so zumindest ein Schluss, der aus einer Studie in Mäusen gezogen werden könnte.38 Dr. Gül Dölen, Forscherin an der Johns Hopkins Universität und Mitglied des MIND Foundation Scientific Advisory Board, sagte hierzu in einem Interview mit dem MIND Blog: „ Jede Substanz oder Manipulation, die eine solche kritische Periode wiedereröffnen kann, hat das Potential therapeutisch wirksam zu sein. Außerdem bedeutet die Abhängigkeit vom therapeutischen Setting, dass Setting und akute psychedelische Erfahrung gemeinsam das Hirn dazu vorbereiten, die richtigen Erinnerungen und Schaltkreise zu reaktivieren sowie diese zur Modifikation in diesem offenen Zustand bereitzustellen.“ Ohne Frage haben all diese Erfahrungen ein neurologisches Korrelat, eine Spur, oder ein „Engramm“, jedoch geschuldet der Komplexität der Gehirnstruktur gibt es keine Technologie, die spezifisch die Schaltkreise, die mit traumatischen Erinnerungen oder schädlichen Verhaltensweisen zusammenhängen, erkennen und ändern kann. Es scheint, als sei das einzige Fenster, welches wir in diese Schaltkreise haben, der Akt der Erinnerung.
In anderen Worten scheinen bestimmte veränderte Bewusstseinszustände (wie die unter dem Einfluss von Psychedelika, aber möglicherweise auch andere Substanzen), im Kontext des therapeutischen Problems, die Kuratoren einer spezifischen nützlichen und unter Umständen beständigen Plastizität zu sein. Ohne solche Erfahrungen jedoch, könnten Psychoplastogene bloß einen vorübergehenden Anstieg willkürlicher Verbindungen im Gehirn bewirken.
Dieser Artikel soll nicht die enormen Leistungen der vielen WissenschaftlerInnen schmälern, welche versuchen nicht-halluzinogene Psychoplastogene zu entwickeln, sondern soll auf neurobiologischer Ebene Argumente für den Nutzen psychedelischer Erfahrung geben. Dies ist von höchster Wichtigkeit, da neurologische Diskurse eine zentrale Rolle in der gesellschaftlichen Diskussion über psychische Gesundheit eingenommen haben, selbst in Situationen, in denen wir noch nicht mal mit Sicherheit sagen können, mit welchen psychischen Prozessen wir es zu tun haben. Hieraus folgt, dass psychiatrische Erkrankungen mit unzureichender Trennschärfe voneinander unterschieden werden, um dann mit neurobiologischen Markern gleichgesetzt zu werden, die es im Folgenden zu korrigieren gilt. Diese Tendenz, angetrieben von einer Pharmaindustrie, in der die Medikamentenentwicklung untrennbar mit Verschreibungslogik und ökonomischen Verwertungsketten verbunden ist, führt dazu, dass vermehrt allzu einfache und marktfähige Lösungen für kaum verstandene Probleme geliefert werden.33
Das Aufkommen psychedelischer Therapien geht für viele mit der Hoffnung einher, dass sie ändern können, wie wir Hirn, Geist und ihre verschiedensten Abweichungen von der Norm verstehen. Psychedelika werden, entgegen dem überschwänglichen Enthusiasmus einiger weniger Parteien, sicher kein Allheilmittel für die bestehende Krise in der Behandlung psychischer Erkrankungen sein. Doch ihre Wiedereinkehr in der klinischen Anwendung hat maßgeblich die menschliche Erfahrung wieder ins Zentrum der Diskussion gebracht – nicht bloß als Ergebnis psychiatrischer Behandlung, sondern auch als Mittel zur Besserung.39
Das Reframing von Psychedelika als Psychoplastogene und der Schritt von der „Korrektur chemischer Ungleichgewichte“ hin zur „Korrektur geschädigter Schaltkreise“, welcher psychedelische Erfahrungen bezichtigt teuer und nicht skalierbar zu sein, verfehlt diesen Schritt zur menschlichen Erfahrung komplett. Niemand wird das transformative Potential der Geburt eines eigenen Kindes, einer Gipfelerfahrung40 oder einer Nahtoderfahrung bestreiten. Viele Menschen vergleichen ihre psychedelischen Erfahrungen mit diesen intensiven Erfahrungen und bewerten sie zudem als einige der Bedeutungsvollsten Erfahrungen ihres Lebens.34
Und während es ein wichtiger Punkt ist, dass PatientInnen in der psychedelischen Therapie besonders viel Aufmerksamkeit und Pflege benötigen, so ist es gegebenenfalls genau das, was diese Menschen brauchen. Diese Ansicht, Pflegebedürfnis als ein teures Ärgernis zu betrachten, das es zu eliminieren gilt, hat uns ein System der sogenannten ‚Managed Care‘41 beschert, in dem Antidepressiva häufig ohne weitere therapeutische Betreuung verschrieben werden und in dem bis zu einem Drittel der PatientInnen nicht ausreichend behandelt werden.33,35 PatientInnen, die klassische Antidepressiva sowie psychedelische Therapie erhalten haben, bekräftigen dieses Urteil: „[Antidepressiva sind] wie wenn man Schmerzmittel für Zahnweh nimmt, man kommt nicht zum Ursprung des Problems“.36 Viele assoziieren klassische Antidepressiva mit der Vermeidung zugrundliegender Ursachen ihrer Depressionen, und empfinden eine sogar noch stärkere Diskonnektion, was im direkten Kontrast zur psychedelischen Therapie steht.36
Für jene, die Einschlusskriterien für eine Behandlung mit psychedelischer Therapie nicht erfüllen, könnten nicht-halluzinogene Psychoplastogene eine reelle Chance zur Besserung sein, vorausgesetzt, dass sie existieren und funktionieren. Falls nicht, so könnten Mikrodosen klassischer Psychedelika eine Alternative darstellen, sofern sich diese Praxis als effektiv in der Behandlung von Depressionen herausstellen sollte. Allerdings scheinen weitere Verschreibung von Pillen und die Rückentlassung von PatientInnen in dasselbe Umfeld zu entlassen, in welchem Sie ihre Depression auch entwickelt haben, keine nachhaltige Lösung zu sein.
Weiterhin besteht das Risiko, dass der Markt Trip-freie Psychedelika als grobe aber eben gerade ausreichende Versionen klassischer Psychedelika annehmen könnte, womit der Trip, mit seinen Komplexitäten und Herausforderungen zur Integration in unser konventionelles Gesundheitssystem wegrationalisiert würde. Was also nun noch als Revolution des Sektors der psychischen Gesundheit erscheint, könnte sich als ein geschicktes Neuverpacken gescheiterter Behandlungsmodelle herausstellen. Wenn aus Psychedelika Psychoplastogene werden, sperrt die Psychiatrie möglicherweise ein weiteres Mal die menschliche Subjektivität aus, gerade in dem Moment, in dem sie behutsam wieder auf Ihren rechtmäßigen Platz zurückkehrt.
Wenn Sie unsere Vision teilen und psychedelische Forschung und Bildung unterstützen wollen, sind wir für jeden Betrag dankbar, den Sie geben können.