Zastrzeżenie: Ten wpis na blogu został przetłumaczony i sprawdzony przez wolontariuszy. Osoby zaangażowane w tłumaczenie nie reprezentują MIND Foundation. Jeśli znajdą Państwo błędy lub niespójności, lub jeśli coś w tłumaczeniu nie jest jasne, prosimy o poinformowanie nas o tym – będziemy wdzięczni za wszelkie poprawki. (mailto:[email protected]) Jeśli chcieliby Państwo pomóc w naszym wielojęzycznym projekcie, prosimy o kontakt w celu dołączenia do Blog Translation Group!
Klauzula o wyłączeniu odpowiedzialności: Każda zmiana w programie terapii z użyciem antydepresantów powinna być skonsultowana z lekarzem lub psychiatrą, w celu zapobiegnięcia zespołowi abstynencyjnemu i ewentualnemu nawrotowi choroby.
W większości najnowszych badań klinicznych z wykorzystaniem substancji psychodelicznych, potencjalni uczestnicy przyjmujący środki antydepresyjne zostali odrzuceni lub poproszeni o zaprzestanie stosowania leków. Niektóre ośrodki wykorzystujące psychodeliki w terapii również przyjmują tylko tych pacjentów, którzy nie zażywają środków przeciwdepresyjnych.
W związku z tym, iż psychodeliki wykazują potencjał w leczeniu przypadków ciężkiej depresji,1,2 ich interakcje z antydepresantami i związane z nimi ryzyko są częstym tematem dyskusji. Ten artykuł ma na celu zbadanie tej kwestii oraz dostarczenie wstępnych odpowiedzi.
Definicja klasycznych psychodelików opiera się na podstawie ich agonistycznego działania na receptory serotoninowe, w szczególności na receptory serotoninowe 2A (5HT2AR).3,4 Podanie antagonistów 5HT2AR, takich jak ketanserina, prowadzi do blokady subiektywnych i biologicznych efektów klasycznych psychodelików.5,6 Badania wykazują, że klasyczne psychodeliki są względnie bezpieczne w kontekście badań klinicznych – mimo istotnych skutków ubocznych, takich jak delikatne bóle głowy, niski wzrost ciśnienia krwi, oraz silne stany lękowe, żadne z nich zazwyczaj nie wymaga interwencji medycznej.2,7,8
Pomimo że dokładny mechanizm działania i farmakokinetyka tych substancji nie jest do końca zrozumiana, dwie poszczególne kwestie związane z ich interakcją ze środkami przeciwdepresyjnymi zostają często poruszane: tak zwany zespół serotoninowy oraz zmniejszenie subiektywnych doświadczeń psychodelicznych.
Do you want to become a psychedelic therapist?
We offer a comprehensive training in psychedelic-augmented psychotherapy for medical doctors and licensed psychotherapists. Learn more and apply here: mind-foundation.org/apt
We also host monthly info meetups where you can meet the faculty and course participants: mind-foundation.org/apt-meetups
ZESPÓŁ SEROTONINOWY: ANTYDEPRESANTY I PSYCHODELIKI
Zespół serotoninowy jest potencjalnie śmiertelną, niepożądaną reakcją na leki , występującą najczęściej, gdy związki chemiczne zwiększające neurotransmisję serotoniny zażywane są jednocześnie. Jednakże, zespół serotoninowy może występować również po zażyciu tylko jednego takiego związku.9 Serotonina syntezowana jest z aminokwasu L-tryptofanu, a jej działania regulowane są przez mechanizmy zwrotnego wychwytu, pętle sprzężenia zwrotnego, oraz enzymy takie jak monooksydaza. Serotonina działa na ośrodkowy oraz obwodowy układ nerwowy. W ośrodkowym układzie nerwowym, wpływa ona m.in. na świadomość, zachowanie, napięcie mięśni i temperaturę ciała. W obwodowym układzie nerwowym, reguluje ona napięcie naczyniowe, nocycepcję (odczuwanie bólu) oraz aktywność żołądka.10 Serotonina działa na 7 rodzin receptorów (od 5-HT1 do 5-HT7) i co najmniej 14 ich podtypów.3
Syndrom serotoninowy odnotowano we wszystkich grupach wiekowych. Szacuje się, że występuje on u 15% osób, u których wystąpiło przedawkowanie selektywnych inhibitorów wychwytu zwrotnego serotoniny (ang. SSRIs). Niemniej jednak, dokładna częstotliwość występowania tego zespołu jest trudna do zweryfikowania, ponieważ jego objawy nie są specyficzne oraz z powodu znikomej świadomości lekarzy na temat tego zespołu. Jedna z ankiet wykazała, że 85% lekarzy nie było świadomych istnienia tego toksydromu.11
Dotkliwość syndromu serotoninowego waha się od łagodnego do zagrażającego życiu. Symptomy często opisywane są jako ‘triada kliniczna,’ czyli zaburzenia nerwowo-mięśniowe (takie jak drżenie lub nadmierne napięcie mięśni prowadzące do hipertermii), nadczynność autonomicznego układu nerwowego (prowadząca do przyspieszenia akcji serca i biegunki) oraz zmiany w stanie psychicznym (takie jak pobudzenie lub majaczenie; rysunek 1).9

Rysunek 1. Spektrum symptomów klinicznych. Objawy zespołu serotoninowego wahają się od łagodnych do zagrażających życiu. Pionowe strzałki wskazują przybliżony punkt, w którym objawy kliniczne początkowo pojawiają się w spektrum choroby, chociaż nie wszystkie zawsze pojawiają się u każdego pacjenta z zespołem serotoninowym. Poważne objawy mogą maskować inne objawy kliniczne. Na przykład hipertoniczność mięśni może maskować drżenie i hiperrefleksję.9
Dokładna patofizjologia zespołu serotoninowego nie jest do końca znana, ale wydaje się ona wynikać z nadmiernej neurotransmisji serotoniny. Nie jest ona nawet powiązana z pojedynczymi receptorami serotoniny, pomimo tego, iż sugeruje się, że receptory 5-HT2A w znacznym stopniu przyczyniają się do powstawania dolegliwości. Wydaje się, że pozostałe receptory, np. 5-HT1A, również odgrywają ważną rolę, szczególnie w przypadkach, gdy stężenia serotoniny osiągają punkt nasycenia wszystkich podtypów receptorów (rysunek 2).11
Inne neuroprzekaźniki, takie jak noradrenalina, również mogą odgrywać rolę w zespole serotoninowym: na przykład wzrost poziomu noradrenaliny w ośrodkowym układzie nerwowym koreluje z występowaniem cięższych objawów.11 Również dopamina może wpływać na proces powstawania objawów – wzrost neurotransmisji dopaminy może pośrednio wywoływać uwalnianie serotoniny.12-14
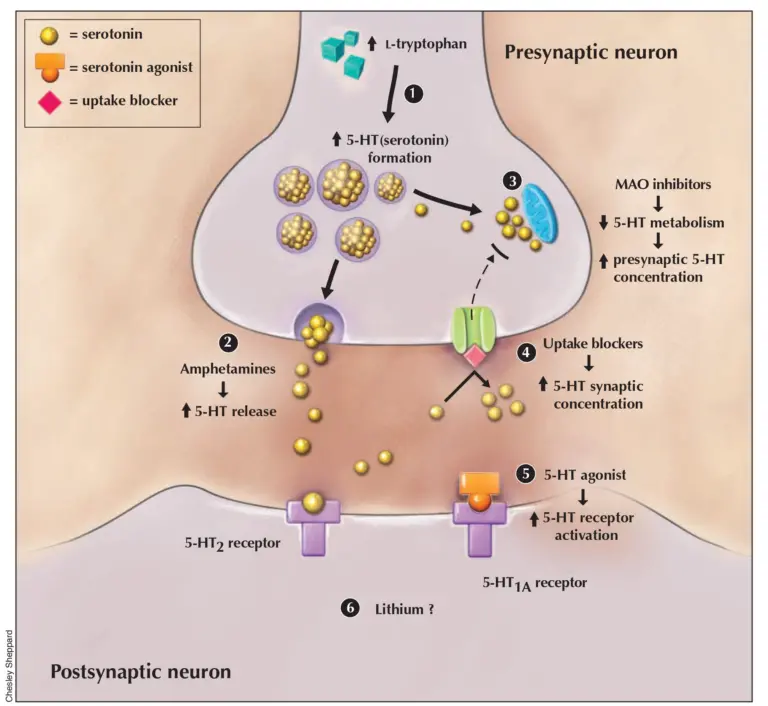
Rysunek 2: Mechanizmy zespołu serotoninowego: 1) Zwiększone dawki L-tryptofanu proporcjonalnie zwiększają syntezę 5-hydroksytryptaminy (5-HT, serotoniny). 2) Amfetaminy i inne leki zwiększają uwalnianie zmagazynowanej serotoniny. 3) Zahamowanie metabolizmu serotoniny przez inhibitory monoaminooksydazy (MAO) zwiększa presynaptyczne stężenie 5-HT. 4) Spadek transportu 5-HT do nerwu presynaptycznego przez blokery wychwytu zwiększa stężenie synaptycznej 5-HT. 5) Bezpośredni agoniści serotoniny mogą stymulować postsynaptyczne receptory 5-HT. 6) Lit zwiększa odpowiedzi receptorów postsynaptycznych. Diament = bloker wychwytu 5-HT; żółte kulki = 5-HT; pomarańczowe kulki = agonista 5-HT o bezpośrednim działaniu. 11
W większości krajów przepisywanie więcej niż jednego leku serotoninowego na raz jest przeciwwskazane, ponieważ może to prowadzić do zespołu serotoninowego. Jak wyszczególniono w tabeli 1 poniżej, każdy lek, który zwiększa neurotransmisję serotoniny, może być zaangażowany w jej patogenezę. Większość przypadków dotyczy leków z grupy SSRI lub inhibitorów monoaminooksydazy (MAOI), przyjmowanych jednocześnie z co najmniej jednym innym lekiem podnoszącym poziom serotoniny. Łączenie leków, które w różny sposób zwiększają neurotransmisję serotoninową, zwiększa prawdopodobieństwo wywołania ciężkiego zespołu serotoninowego.15

Tabela 1: Leki związane z zespołem serotoninowym. 9 1) SSRI. 2) Antydepresanty. 3) MAOI. 4) Leki przeciwpadaczkowe. 5) Leki przeciwbólowe. 6) Leki przeciwwymiotne. 7) Leki przeciwmigrenowe. 8) Leki na otyłość. 9) Antybiotyki. 10) Leki bez recepty. 11) Narkotyki.
Do tej pory nie ma jeszcze danych empirycznych na temat interakcji między psychodelikami a lekami przeciwdepresyjnymi oraz ich wpływu na ryzyko pojawienia się zespołu serotoninowego. Wiadomo jednak, że psychodeliki są agonistami receptorów 5-HT2A, a zatem zwiększają ich neurosygnalizację. Z farmakologicznego punktu widzenia jest więc prawdopodobne, że jednoczesne przyjmowanie psychodelików z serotoninergicznymi lekami przeciwdepresyjnymi może wywołać zespół serotoninowy. W związku z tym, łączenie psychodelików z jakimikolwiek lekami, które zwiększają neurotransmisję serotoninergiczną, może być niebezpieczne, zwłaszcza w przypadku zawierającej MAO-I ayahuasce.
Enzym wątrobowy CYP2D6, który metabolizuje niektóre psychodeliki takie jak LSD i 5-Meo-DMT,16,17 bierze również udział w metabolizmie innych substancji, w tym SSRI, które są zarówno substratem jak i inhibitorem tego enzymu.18 Oznacza to, że CYP2D6 nie jest wystarczająco dostępny do metabolizowania zarówno psychodelików, jak i SSRI, co przyczynia się do wzrostu stężenia substancji serotoninergicznych we krwi i może prowadzić do występowania zespołu serotoninowego.11
Z tego powodu zaleca się zmniejszenie dawki leków przeciwdepresyjnych przed podjęciem jakiejkolwiek terapii psychodelicznej lub zażyciem substancji psychodelicznych. Ponadto, w związku z tym, że podawanie środków serotoninowych w ciągu pięciu tygodni po odstawieniu SSRI może wywołać zespół serotoninowy,11 bezpieczniejszym wydaje się odczekanie co najmniej pięciu tygodni przed zażyciem jakiegokolwiek związku psychodelicznego.
LEKI PRZECIWDEPRESYJNE OSŁABIAJĄ SUBIEKTYWNE EFEKTY PSYCHODELICZNE
Oprócz ryzyka wystąpienia zespołu serotoninowego, łączenie psychodelików z lekami przeciwdepresyjnymi może zmienić subiektywne odczucia związane z doświadczeniami psychodelicznymi. Anegdotyczne dowody sugerują, że stosowanie SSRI, jak i przewlekłe stosowanie trójcyklicznych leków przeciwdepresyjnych, może zmienić subiektywne efekty psychodelików. Jeśli chodzi o trójcykliczne leki przeciwdepresyjne, efekt ten może być związany z uwrażliwieniem receptora postsynaptycznego i zwiększonym poziomem dopaminy, co pośrednio prowadzi do zwiększenia neurotransmisji serotoniny.12,13
Badania wykazują, że przewlekłe podawanie SSRI lub MAOI prowadzi do zmniejszenia subiektywnych efektów psychodelików. Przewlekłe podawanie leków z grupy SSRI powoduje obniżenie ekspresji receptorów 5-HT2AR; to z kolei może sprawić, że dana osoba stanie się mniej wrażliwa na substancje wpływające na te receptory, takie jak psychodeliki. Dlatego właśnie spadek subiektywnych efektów może wynikać z obniżenia ekspresji receptorów 5-HT2AR. W przypadku MAOI badania wykazują, że ich przewlekłe podawanie powoduje uniewrażliwienie receptora serotoninowego, co może wyjaśniać obserwowany spadek subiektywnych efektów psychedelicznych.19,20,21
Dokładne mechanizmy leżące u podstaw modulacji doświadczenia psychodelicznego przez leki przeciwdepresyjne są nadal niejasne i należy przeprowadzić dalsze badania w celu uzyskania lepszego zrozumienia. Ponadto, ryzyko zespołu serotoninowego nie powinno być ignorowane mimo obserwacji zaburzenia subiektywnych efektów psychodelików po zredukowaniu ekspresji 5-HT2AR.
Możliwe, że zespół serotoninowy zależy od wskaźnika zajęcia receptorów 5-HT, przy czym wyższy wskaźnik zajętych receptorów można łatwiej osiągnąć, gdy ogólna liczba receptorów zostanie zmniejszona. Co więcej, kilka różnic międzyosobniczych, takich jak zmiany genetyczne w enzymach odpowiedzialnych za metabolizm leków, również może odgrywać rolę w występowaniu zespołu serotoninowego. 22
KILKA MYŚLI KOŃCOWYCH
Nie można z całkowitą pewnością stwierdzić, jaki jest związek pomiędzy zespołem serotoninowym a farmakologią psychodelików. Nasza obecna wiedza jest niewystarczająca do sformułowania dokładnej oceny ryzyka lub modelu modulacji zarówno subiektywnych, jak i fizjologicznych skutków wynikających z połączenia leków przeciwdepresyjnych i substancji psychodelicznych.
W ostatnich latach nie odnotowano dużego postępu w wyjaśnianiu patofizjologii zespołu serotoninowego. Ponieważ dzięki badaniom naukowym uzyskujemy jaśniejszy pogląd na farmakologię psychodelików, opracowanie bardziej precyzyjnych zaleceń dotyczących pracy klinicznej w przyszłości powinno stać się priorytetem.
Niemniej jednak, szczegółowa ocena wpływu powszechnych leków przeciwdepresyjnych i psychodelicznych na neurotransmisję serotonergiczną sugeruje, że ta kombinacja jest ryzykowna z farmakologicznego punktu widzenia i mało prawdopodobne jest, aby miała ona klinicznie korzystne skutki. W związku z tym, zaleca się ostrożność przy rozważaniu przyjmowania psychodelików podczas przyjmowania leków przeciwdepresyjnych.
Integration is key to bring positive change into our lives. That requires patience and the right tools. Our Beyond Experience workshops provide not just that, but also a great chance to network and learn together with people on a similar path.
What’s more, Beyond Experience takes place in many locations across Europe!
Learn more and sign up here: mind-foundation.org/beyond-experience
![]() English
English
![]() German
German
![]() Dansk
Dansk
![]() Français
Français
![]() עברית
עברית
![]() Italiano
Italiano
![]() Português
Português
![]() Русский
Русский
![]() Español
Español
![]() Svenska
Svenska
![]() Ελληνικα
Ελληνικα
![]() فارسی
فارسی










