Disclaimer: This blog post translation has been contributed and reviewed by volunteers. The contributors do not represent the MIND Foundation. If you find mistakes or inconsistencies, or if something in the translation seems unclear, please let us know – we are thankful for any improvements.
If you want to help with your linguistic skills, please write to the same link and join the blog post translators!
Дисклеймер: перед тем, как вносить изменения в схемы приема антидепрессантов, пациенты должны обязательно проконсультироваться с терапевтом или психиатром, чтобы предотвратить синдром отмены и дальнейший рецидив.
Принимающие антидепрессанты испытуемые делают паузу в лечении или вовсе не участвуют в тестах — таковы условия недавно проведенных клинических исследований психоделических препаратов. Аналогично, психоделические ретриты допускают только тех пациентов, которые в настоящий момент не принимают антидепрессанты.
В связи с тем, что психоделикам удалось дать надежду в лечении тяжелых форм депрессии[1] [2], теперь возникает очевидное беспокойство относительно потенциальных рисков в их взаимодействии с антидепрессантами. Целью данной статьи является изучение изложенной выше проблемы и описание некоторых предварительных заключений.
Классические психоделики определяет их способность действовать как агонисты рецепторов серотонина, в частности рецептора серотонина 2А (5HT2AR)[3] [4]. Соответственно, многие субъективные и биологические эффекты классических психоделиков блокируются после введения антагонистов 5HT2AR, таких, как кетансерин[5] [6]. В контексте клинических исследований классические психоделики оказались относительно безопасными; с побочными эффектами, не требующими медицинского вмешательства: умеренными головными болями, небольшим повышением кровяного давления, тревожностью[7] [8]. Несмотря на то, что точные механизмы действия и фармакокинетику этих молекул еще не удалось определить, мы сталкиваемся с двумя основными проблемами относительно их взаимодействия с антидепрессантами: т.н. серотониновый синдром и снижение психоделических эффектов.
Do you want to become a psychedelic therapist?
We offer a comprehensive training in psychedelic-augmented psychotherapy for medical doctors and licensed psychotherapists. Learn more and apply here: mind-foundation.org/apt
We also host monthly info meetups where you can meet the faculty and course participants: mind-foundation.org/apt-meetups
Серотониновый синдром: антидепрессанты и психоделики
Серотониновый синдром является потенциально летальной побочной реакцией на одновременное употребление тех препаратов, которые способны усилить нейротрансмиссию серотонина. Однако подобная реакция возможна и после употребления одного из таких веществ[9]. Серотонин производится из аминокислоты L-триптофана, и его эффекты регулируются механизмами обратного захвата, петлями обратной связи и ферментами, такими, как моноаминоксидаза. Серотонин влияет на нервную систему как на центральном, так и на периферийном уровнях. В центральной нервной системе он воздействует на сознание, поведение, мышечный тонус, температуру тела и боль. В периферийной нервной системе он регулирует тонус мышц, ноцицепцию (восприятие боли) и желудочную активность[10]. Эффекты серотонина опосредованы рецепторами 7 типов (от 5-HT1 до 5-HT7) и не менее 14 подтипов.
Серотониновый синдром наблюдается среди всех возрастных групп и случается у 15% процентов людей, испытавших передозировку СИОЗС (Селективных ингибиторов обратного захвата серотонина).
Однако в связи с размытыми симптомами и недостаточной осведомленностью врачей, точные данные по числу инцидентов серотонинового синдрома сложно получить. Проведенный опрос показал, что 85% врачей не знают о существовании этого вида интоксикации[11].
Выраженность серотонинового синдрома может варьироваться от легкой до угрожающей жизни. Его симптомы часто изображаются в виде клинической триады: нервно-мышечные нарушения (такие, как тремор или мышечный гипертонус, за которым следует гипертермия), гиперактивность вегетативной нервной системы (приводит к учащению пульса и диарее) и изменения психического состояния (например, возбуждение или делирий; см. обзор на Изображении 1).

Изображение 1: Спектр клинических симптомов: Проявления серотонинового синдрома варьируются от легких до опасных для жизни. Вертикальные стрелки указывают приблизительную точку, в которой клинические показатели первоначально появляются в спектре заболевания, хотя не все характеристики всегда проявляются у одного пациента с серотониновым синдромом. Тяжелые симптомы могут маскировать другие клинические показатели. Например, мышечный гипертонус может подавить тремор и гиперрефлексию.
Точная патофизиология серотонинового синдрома до конца не изучена, но, по-видимому, он случается в результате избытка нейротрансмиссии серотонина. Он связан не только с рецептором серотонина, хотя предполагается, что рецепторы 5-HT2A вносят существенный вклад в это состояние. Другие рецепторы, такие, как 5-HT1A, по-видимому, также способствуют этому. Это происходит, когда концентрации серотонина достигают той точки, в которой все другие подтипы рецепторов поглощаются (см. Изображение 2). Другие нейротрансмиттеры, такие как норадреналин, также могут играть важную роль в этом синдроме: например, повышение концентрации норадреналина в ЦНС во время серотонинового синдрома коррелирует с более тяжелыми симптомами. В этом может быть задействован и дофамин, поскольку усиление нейротрансмиссии дофамина способно косвенно спровоцировать высвобождение серотонина[12] [13] [14].
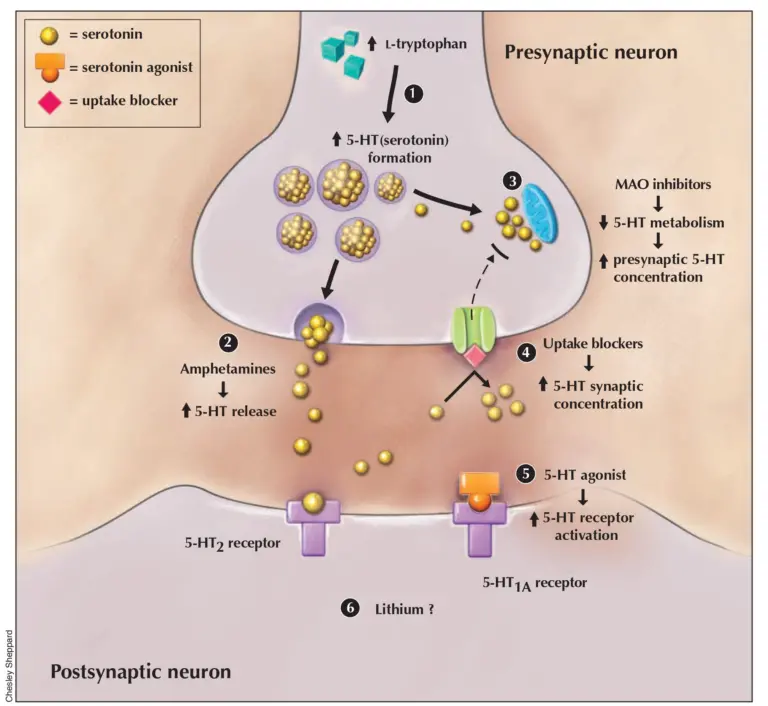
Изображение 2: Механизмы серотонинового синдрома: 1) Повышенные дозы L-триптофана пропорционально усиливают образование 5-гидрокситриптамина (5-HT или серотонина). 2) Амфетамины и другие препараты усиливают высвобождение накопленного серотонина. 3) Ингибирование метаболизма серотонина ингибиторами моноаминоксидазы (МАО) увеличивает пресинаптическую концентрацию 5-HT. 4) Нарушение транспортировки 5-HT в пресинаптический нерв блокаторами захвата увеличивает синаптическую концентрацию 5-HT. 5) Прямые агонисты серотонина могут стимулировать постсинаптические 5-HT рецепторы. 6) Литий усиливает ответную реакцию постсинаптических рецепторов. Ромб = препарат блокирования 5-HT поглощения; закрашенные кружки = 5-HT; звездочка = агонист 5-HT прямого действия.
В большинстве стран во избежание серотонинового синдрома противопоказано назначение более одного серотонинового препарата. Как подробно описано в Таблице 1 ниже, каждое лекарство, которое усиливает нейротрансмиссию серотонина, может участвовать в его патогенезе. Большинство случаев включают одновременное употребление СИОЗС или ИМАО (ингибиторы моноаминоксидазы) и другого препарата, повышающего уровень серотонина. Комбинирование препаратов, дифференцированно усиливающих нейротрансмиссию серотонина, с большей вероятностью может вызвать тяжелый серотониновый синдром[15].

Таблица 1: Препараты, связанные с серотониновым синдромом
В настоящий момент отсутствуют эмпирические данные о взаимодействии психоделиков и антидепрессантов, а также о рисках возникновения серотонинового синдрома при их взаимодействии. Однако мы точно знаем, что психоделики обладают свойствами агонистов 5-HT2AR, что усиливает нейротрансмиссию 5-HT2AR. Таким образом, с фармакологической точки зрения кажется вероятным, что их совместное применение с серотонинергическими антидепрессантами может вызвать серотониновый синдром. Соответственно, сочетание психоделиков и любых препаратов, усиливающих серотонинергическую нейротрансмиссию, потенциально опасно.
Не менее важно отметить, что некоторые психоделики, такие, как ЛСД и 5-Мео-ДМТ, метаболизируются ферментом печени CYP2D6[16] [17], который участвует в метаболизме и других веществ. Вместе с тем, СИОЗС являются как субстратом, так и ингибитором этого фермента[18]. Это означает, что CYP2D6 плохо справляется с одновременным метаболизмом психоделиков и СИОЗС. Это приводит к увеличению концентрации серотонинергических веществ в крови, что является возбудителем серотонинового синдрома.
По описанной причине перед началом психоделической терапии или рекреационного употребления психоделиков рекомендуется сократить прием антидепрессантов. Более того, поскольку было показано, что введение агентов, высвобождающих серотонин, в течение пяти недель после прекращения приема СИОЗС вызывает серотониновый синдром, представляется более безопасным подождать не менее пяти недель перед употреблением психоделических препаратов.
Антидепрессанты притупляют субъективные эффекты психоделиков
Помимо риска серотонинового синдрома, сочетание психоделиков и антидепрессантов может привести к изменению субъективных эффектов психоделического опыта. Неофициальные данные свидетельствуют о том, что кратковременное употребление СИОЗС или длительное употребление трициклических антидепрессантов ведет к изменению субъективных эффектов психоделиков. Касаемо трициклических антидепрессантов это наблюдение может быть связано с сенсибилизацией постсинаптических рецепторов и повышенным уровнем дофамина, что косвенно приводит к усилению нейротрансмиссии серотонина.
Напротив, при длительном употреблении СИОЗС или ИМАО было обнаружено ослабление субъективных эффектов психоделиков. Возможной причиной относительно СИОЗС может быть то, что хронический прием СИОЗС провоцирует подавление рецепторов 5-HT2AR. Это в свою очередь может ослабить чувствительность к веществам, влияющим на данные рецепторы: например, к психоделикам. Соответственно, такое ослабление субъективных реакций может быть вызвано подавлением 5-HT2AR. Длительный прием препаратов ИМАО провоцирует десенсибилизацию серотониновых рецепторов, что может объяснить наблюдаемое ослабление субъективных эффектов психоделиков[19] [20] [21].
Точные механизмы, лежащие в основе изменения психоделического опыта антидепрессантами, все еще неясны, и для лучшего понимания этих процессов необходимо провести дальнейшие исследования. Кроме того, во время изучения притупленных субъективных эффектов психоделиков при подавлении 5-HT2AR не стоит забывать о риске серотонинового синдрома. В частности, возможно, что серотониновый синдром зависит от количества оккупированных рецепторов 5-HT, в результате чего более высокий уровень оккупированных рецепторов может быть легче достигнут, когда общее количество рецепторов снижено. Кроме того, такие индивидуальные колебания, как генетические вариации ферментов, ответственных за метаболизм лекарств, также могут играть роль в возникновении серотонинового синдрома[22].
Заключительные соображения
В данный момент невозможно точно определить связь между серотониновым синдромом и фармакологическими свойствами психоделиков. Текущих знаний недостаточно для формулирования точной оценки риска или построения модели модуляции как субъективных, так и физиологических эффектов, возникающих в результате комбинации антидепрессантов и психоделических веществ.
В течение последних лет ощутимого прогресса в выявлении патофизиологии серотонинового синдрома не наблюдалось. Однако фармакологические свойства психоделиков становятся для нас всё более очевидными, поэтому в ближайшем будущем, вероятно, удастся разработать более четкие рекомендации для клинической работы.
Вместе с тем, пристальное изучение воздействия антидепрессантов и психоделических препаратов на нейротрансмиссию серотонина позволяет предположить, что подобная комбинация обладает повышенным риском с фармакологической точки зрения и с малой вероятностью будет иметь клинические преимущества. Следовательно, рекомендуется с осторожностью принимать психоделики во время лечения антидепрессантами.
Integration is key to bring positive change into our lives. That requires patience and the right tools. Our Beyond Experience workshops provide not just that, but also a great chance to network and learn together with people on a similar path.
What’s more, Beyond Experience takes place in many locations across Europe!
Learn more and sign up here: mind-foundation.org/beyond-experience
![]() English
English
![]() German
German
![]() Dansk
Dansk
![]() Français
Français
![]() עברית
עברית
![]() Italiano
Italiano
![]() polski
polski
![]() Português
Português
![]() Español
Español
![]() Svenska
Svenska
![]() Ελληνικα
Ελληνικα
![]() فارسی
فارسی










